Risicominimalisatie-materialen betreffende selexipag voor voorschrijvers
|
|
|
- David Maes
- 5 jaren geleden
- Aantal bezoeken:
Transcriptie
1 Risicominimalisatie-materialen betreffende selexipag voor voorschrijvers januari 208 Geachte voorschrijver, In overleg met het College ter Beoordeling van Geneesmiddelen willen wij u graag informeren over additionele risicominimalisatie-materialen voor selexipag, een selectieve IP-receptoragonist. Deze materialen bevatten aanbevelingen om belangrijke risico s van dit geneesmiddel te beperken of te voorkomen. Selexipag is geïndiceerd voor de langdurige behandeling van pulmonale arteriële hypertensie bij volwassen patiënten met WHO-functionele klasse II-III, hetzij als combinatietherapie bij patiënten die onvoldoende onder controle zijn te brengen met een endothelinereceptorantagonist en/ of een fosfodiësterase type -remmer, hetzij als monotherapie bij patiënten die niet voor deze behandelingen in aanmerking komen. Samenvatting Selexipag is beschikbaar in tabletten van, 400, 00, 800, 000, 00, 00 en 00. Iedere patiënt moet worden getitreerd naar de hoogste persoonlijk verdraagbare dosis waarbij de aanvangsdosis van ongeveer wekelijks met wordt verhoogd. Om medicatiefouten te voorkomen worden tijdens de titratie tabletten van en 800 gebruikt. De patiënt neemt s morgens en s avonds een dosis in, startend met een avonddosis. Wanneer de dosis verhoogd wordt, zal de eerste hogere dosis ook weer s avonds worden ingenomen. Pas nadat de persoonlijke onderhoudsdosering is vastgesteld, kan tweemaal daags één enkele tablet met de geschikte sterkte worden voorgeschreven. Bespreek en overhandig de titratiegids voor patiënten aan de patiënt. Om het risico van medicatiefouten te verminderen als gevolg van de noodzaak om tijdens het optitreren meerdere tabletten van maximaal 2 verschillende sterktes te gebruiken, zijn de bijgevoegde risicominimalisatie-materialen ontwikkeld: Een gelamineerde A4-kaart Titratiegids selexipag voor de voorschrijver waarop staat: Het titratieschema en uitleg over de dosering van selexipag. Productinformatie, bestaande uit: De samenvatting van de productkenmerken (SmPC). De titratiegids voor patiënten en de bijsluiter: Deze gids en de bijsluiter zijn bedoeld om aan de patiënt te laten zien en om veilig en effectief gebruik van selexipag met de patiënt te bespreken. Na afloop van het consult dient alleen de titratiegids aan de patiënt te worden meegegeven. NB: patiënten zullen een identieke titratiegids en de patiëntenbijsluiter ontvangen in de titratieverpakking. U kunt extra materiaal opvragen via localinfo.nlwo@its.jnj.com. Aanvullende informatie betreffende selexipag is beschikbaar in de SmPC en bijsluiter op Het additioneel risicominimalisatie-materiaal is online beschikbaar op PH-8-09 v3 - januari 208
2 Meld bijwerkingen bij het Nederlands Bijwerkingencentrum Lareb Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe veiligheidsinformatie worden vastgesteld. Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico s van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via het Nederlands Bijwerkingencentrum Lareb; website Met vriendelijke groet, Pharmaceuticals Nederland B.V. Han Brouwer, General Manager Suzanne Jansen, Medical Director PH-8-09 v3 - januari 208
3 Risicominimalisatie-materiaal over de risico s van selexipag voor voorschrijvers. Dit materiaal beschrijft aanbevelingen om belangrijke risico s van selexipag te beperken of te voorkomen. Het materiaal is beoordeeld door het College ter Beoordeling van Geneesmiddelen (CBG). Selexipag is beschikbaar als tabletten van, 400, 00, 800, 000, 00, 00 en 00. Titratiekaart selexipag voor de voorschrijver Titratiefase: Het doel van de titratie is om voor elke patiënt individueel de meest geschikte dosis te bereiken. Dit gebeurt gewoonlijk binnen 8 weken. Om u te helpen tijdens het titratieproces, en om het risico van medicatiefouten te verminderen als gevolg van de noodzaak om tijdens het optitreren meerdere tabletten van maximaal 2 verschillende sterktes ( en 800 ) te gebruiken is onderstaand schema opgesteld. tablet 800 tablet Titratieverpakking ) Start met tweemaal daags elke uur. Neem de tabletten in met voedsel om de verdraagbaarheid te verbeteren.de eerste tablet moet s avonds ingenomen worden Titreer met zo weinig mogelijk tabletten 2) Bij een benodigde dosis hoger dan 800 ontvangt de patiënt: Nog een titratieverpakking van tabletten Een verpakking van 800 tabletten Bij controle van de patiënt Verhoog de dosis tot bijwerkingen optreden die niet verdragen worden 3) of niet behandelbaar zijn Maximale dosis De maximale dosis die aan een patiënt gegeven mag worden is tweemaal daags 00 Optitreren Verhoog de dosis met tweemaal daags. Elke dosisstap duurt ongeveer week. Bij elke stap moet de eerste dosis s avonds ingenomen worden Stap terug Verlaag de dosis naar het voorgaande niveau als een patiënt de dosis bereikt die niet wordt verdragen of niet behandelbaar is Onderhoudsfase De hoogste verdraagbare dosis wordt de persoonlijke onderhoudsdosis en kan vervangen worden door tweemaal daags een enkele tablet met overeenkomstige sterkte. De dosis mag nooit hoger zijn dan tweemaal daags 00 (Tabletten zijn niet op ware grootte) ) De titratieverpakking bevat 0 filmomhulde tabletten van. Dit zijn voldoende tabletten om tot en met 800 tweemaal daags op te titreren. 2) De 2 verpakkingen bevatten voldoende tabletten om tot en met 00 op te titreren. 3) De meest voorkomende bijwerkingen die uw patiënt kan ervaren tijdens het gebruik van selexipag zijn: hoofdpijn, diarree, misselijkheid en braken, kaakpijn, spierpijn, pijn in de extremiteiten, gewrichtspijn en overmatig blozen. Voor een volledige lijst van bijwerkingen, zie de SmPC. Raadpleeg de volledige Samenvatting van de productkenmerken (SmPC).
4 Het begin van de behandeling Behandeling met selexipag mag alleen worden ingesteld en gecontroleerd door een arts die ervaren is in de behandeling van PAH De titratieverpakking bevat: filmomhulde tabletten (0 stuks) om te titreren. Een titratiegids voor de patiënt met uitleg over het titratieproces. Hierin is een titratiedagboek opgenomen waarin de patiënt het aantal tabletten noteert dat per dag ingenomen wordt. Neem bij het begin van de behandeling de titratiegids met de patiënt door, om er zeker van te zijn dat de patiënt het titratieproces volledig begrijpt en erop voorbereid is dat er bijwerkingen op kunnen treden. Opmerking: Bij een benodigde dosis hoger dan 800 ontvangt de patiënt nog een titratieverpakking van filmomhulde tabletten (0 stuks) en een verpakking van 800 filmomhulde tabletten (0 stuks) om het aantal tabletten te minimaliseren. Communicatie met de patiënt Neem tijdens de titratieperiode wekelijks contact op met de patiënt om de voortgang te bespreken en om er zeker van te zijn dat bijwerkingen, gerelateerd aan selexipag, adequaat behandeld worden. Bijwerkingen gerelateerd aan selexipag, zoals hoofdpijn, diarree, kaakpijn, misselijkheid, spierpijn, braken, pijn in de extremiteiten, overmatig blozen en gewrichtspijn werden voornamelijk tijdens de titratiefase vaak waargenomen. De verwachte bijwerkingen zijn doorgaans van voorbijgaande aard of beheersbaar met symptomatische behandeling. In de klinische praktijk zijn gastro-intestinale bijwerkingen waargenomen die reageerden op geneesmiddelen tegen diarree, braken en misselijkheid en/of geneesmiddelen voor functionele gastro-intestinale aandoeningen. Bijwerkingen geassocieerd met pijn werden vaak behandeld met analgetica (zoals paracetamol). Onderhoudsfase Zodra de onderhoudsdosis is bereikt kan een enkele tablet met overeenkomstige sterkte voorgeschreven worden voor de persoonlijke onderhoudsdosis (er zijn tabletten beschikbaar van - 00 ). Hierdoor nemen patiënten s avonds tablet en s morgens tablet in. Elke patiënt is verschillend en niet iedereen zal op dezelfde onderhoudsdosis uitkomen. De dosis mag nooit hoger zijn dan tweemaal daags 00. De enkelvoudige tabletten voor de onderhoudsdosis hebben verschillende kleuren en inscripties die de sterkte aanduiden (in honderden men) V3 - aug 208 PH-8- Aanvullende informatie betreffende selexipag is beschikbaar in de Samenvatting van productkenmerken (SmPC) en bijsluiter op Het additioneel risicominimalisatie-materiaal is online beschikbaar op Meld bijwerkingen bij het Nederlands Bijwerkingencentrum Lareb Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe veiligheidsinformatie worden vastgesteld. (Tabletten zijn niet op ware grootte) Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico s van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via het Nederlands Bijwerkingencentrum Lareb; website
5 filmomhulde tabletten Titratiegids Starten van de behandeling met Uptravi Lees de bijgevoegde patiëntenbijsluiter alvorens de behandeling te starten pp0.indd 9.. :3 Format/dimensions 0 x mm Page of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
6 2 Inhoud Hoe moet u Uptravi innemen? Hoe moet u de dosis ophogen? Wat houden de stappen in? Wanneer moet de dosis worden verlaagd? Stap terug pp0.indd :3 Format/dimensions 0 x mm Page 2 of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
7 3 Wanneer u overstapt naar uw onderhoudsdosis..... Bent u vergeten dit middel in te nemen? Als u stopt met het innemen van dit middel Titratiedagboek pp0.indd :3 Format/dimensions 0 x mm Page 3 of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
8 Hoe moet u Uptravi innemen? 4 Uptravi is een geneesmiddel dat elke ochtend en avond moet worden ingenomen voor de behandeling van pulmonale arteriële hypertensie, ook wel PAH genoemd. De aanvangsdosis van Uptravi is eenmaal s ochtends en eenmaal s avonds. De eerste dosis van Uptravi moet s avonds worden ingenomen. U moet elke dosis met een glas water innemen, bij voorkeur tijdens een maaltijd pp0.indd :3 Format/dimensions 0 x mm Page 4 of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
9 Er zijn 2 behandelingsfasen met Uptravi: Titratie De eerste paar weken werkt u samen met uw arts om uit te vinden welke Uptravi-dosis geschikt is voor u. Uw arts zal mogelijk zeggen dat u van de aanvangsdosis naar een hogere dosis Uptravi moet overstappen. Uw arts kan u ook laten overstappen naar een lagere dosis. Dit proces wordt titratie genoemd. Hierdoor kan uw lichaam zich langzaam instellen op het geneesmiddel. Onderhoud Zodra uw arts de dosis heeft gevonden die goed is voor u, zal dit de dosis worden die u blijft innemen. Dit wordt de onderhoudsdosis genoemd pp0.indd 9.. :3 Format/dimensions 0 x mm Page of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
10 Hoe moet u de dosis ophogen? U start met de dosis van s ochtends en s avonds en na overleg met uw arts of verpleegkundige stapt u over naar de volgende hogere dosis. De eerste verhoogde dosis moet u s avonds innemen. Meestal duurt elke stap ongeveer week. Het vinden van de voor u geschikte dosis kan een paar weken duren. Het doel is de dosis te bereiken die het meest geschikt is voor uw behandeling. Deze dosis wordt uw onderhoudsdosis pp0.indd 9.. :3 Format/dimensions 0 x mm Page of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
11 Iedere patiënt met PAH is anders. Niet iedereen komt uit op dezelfde onderhoudsdosis. Sommige patiënten gebruiken als onderhoudsdosis s ochtends en s avonds, terwijl andere patiënten de hoogste dosis van 00 s ochtends en s avonds bereiken. Weer anderen hebben een onderhoudsdosis hier ergens tussenin. Waar het om gaat, is dat u de dosis bereikt die het meest geschikt is voor uw behandeling pp0.indd 9.. :3 Format/dimensions 0 x mm Page of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
12 Wat houden de stappen in? Elke dosisstap duurt ongeveer week. tablet van 8 STARTDOSIS STAP Ochtend: één tablet van Avond: één tablet van (totale dagelijkse dosis: 400 ) STAP 2 Ochtend: twee tabletten van Avond: twee tabletten van (totale dagelijkse dosis: 800 ) STAP 3 Ochtend: drie tabletten van Avond: drie tabletten van (totale dagelijkse dosis: 00 ) STAP 4 Ochtend: vier tabletten van Avond: vier tabletten van (totale dagelijkse dosis: 00 ) pp0.indd :3 Format/dimensions 0 x mm Page 8 of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
13 tablet van 800 (Gebruiken bij stap tot en met 8 om het aantal benodigde tabletten per dosis te verminderen.) tablet van HOOGSTE DOSIS 9 STAP Ochtend: één tablet van 800 en één tablet van Avond: één tablet van 800 en één tablet van (totale dagelijkse dosis: 0 ) STAP Ochtend: één tablet van 800 en twee tabletten van Avond: één tablet van 800 en twee tabletten van (totale dagelijkse dosis: 2400 ) STAP Ochtend: één tablet van 800 en drie tabletten van Avond: één tablet van 800 en drie tabletten van (totale dagelijkse dosis: 2800 ) STAP 8 Ochtend: één tablet van 800 en vier tabletten van Avond: één tablet van 800 en vier tabletten van (totale dagelijkse dosis: 3 ) (Tabletten zijn niet op ware grootte.) pp0.indd :3 Format/dimensions 0 x mm Page 9 of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
14 Wanneer moet de dosis worden verlaagd? Zoals bij alle geneesmiddelen is het mogelijk dat u met Uptravi last krijgt van bijwerkingen wanneer u naar hogere doses overstapt. Overleg met uw arts of verpleegkundige als u last krijgt van bijwerkingen. Er zijn behandelingen beschikbaar die kunnen helpen om ze te verlichten. De meest voorkomende bijwerkingen van Uptravi (kunnen optreden bij meer dan op de 0 mensen) zijn: hoofdpijn diarree misselijkheid braken kaakpijn spierpijn pijn in een been gewrichtspijn roodheid van het gezicht. Zie voor meer informatie de bijsluiter voor een volledige lijst met bijwerkingen pp0.indd :3 Format/dimensions 0 x mm Page 0 of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
15 Als u de bijwerkingen niet verdraagt, zelfs niet nadat uw arts of verpleegkundige heeft geprobeerd ze te behandelen, kan hij of zij u adviseren een stap terug te gaan naar een lagere dosis. Als uw arts of verpleegkundige zegt dat u een stap terug moet naar een lagere dosis, moet u s ochtends en s avonds één tablet van minder innemen. U moet alleen een lagere dosis innemen na overleg met uw PAH-arts of -verpleegkundige. Dit proces van dosisverlaging helpt u de dosis te vinden die geschikt is voor u, de zogeheten onderhoudsdosis pp0.indd 9.. :3 Format/dimensions 0 x mm Page of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
16 Stap terug Elke dosisstap duurt ongeveer week. START STAP STAP 2 STAP 3 tablet van (Tabletten zijn niet op ware grootte.) Ochtend: één tablet van Avond: één tablet van (totale dagelijkse dosis: 400 ) Verhoog uw dosis ongeveer elke week door één tablet van toe te voegen aan uw ochtenden avonddosis pp0.indd 9.. :3 Format/dimensions 0 x mm Page of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
17 VERHOGING STAP TERUG ONDERHOUDSDOSIS STAP 4 STAP STAP TERUG NAAR STAP EEN ENKELE TABLET, ZELFDE DOSIS Het doel is om de hoogste dosis te bereiken met bijwerkingen die u kunt verdragen Stap terug indien de bijwerkingen niet te verdragen zijn Start met de inname van uw hoogste verdraagbare dosis in de vorm van een enkele tablet tablet van tablet van 800 (Gebruiken bij stap tot en met 8 om het aantal benodigde tabletten per dosis te verminderen.) pp0.indd 9.. :3 Format/dimensions 0 x mm Page of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
18 Wanneer u overstapt naar uw onderhoudsdosis De hoogste dosis die u tijdens de titratie verdraagt, wordt uw onderhoudsdosis. Uw onderhoudsdosis is de vaste dosis die u moet blijven innemen. Uw arts of verpleegkundige kan een enkele tablet met die sterkte voorschrijven voor uw onderhoudsdosis. Hierdoor hoeft u s ochtends en s avonds slechts één tablet in te nemen in plaats van een aantal tabletten per keer pp0.indd 9.. :3 Format/dimensions 0 x mm Page of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
19 Als uw hoogste verdraagbare dosis tijdens de titratie bijvoorbeeld 00 s ochtends en s avonds was: Hoogste verdragen dosis Onderhoudsdosis Ochtend Hoogste verdragen dosis Onderhoudsdosis Avond Het kan zijn dat uw arts of verpleegkundige na verloop van tijd uw onderhoudsdosis indien nodig aanpast pp0.indd 9.. :3 Format/dimensions 0 x mm Page of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
20 Bent u vergeten dit middel in te nemen? Als u bent vergeten een dosis in te nemen, moet u die dosis innemen zodra u eraan denkt en daarna uw tabletten op de gebruikelijke tijdstippen blijven innemen. Als het minder dan uur is tot u normaal uw volgende dosis zou innemen, moet u de gemiste dosis overslaan en uw geneesmiddel innemen op het normale tijdstip. Neem geen dubbele dosis om een vergeten tablet in te halen pp0.indd 9.. :3 Format/dimensions 0 x mm Page of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
21 Als u stopt met het innemen van dit middel Stop niet met het innemen van Uptravi tenzij dat van uw arts of verpleegkundige moet. Als u om welke reden dan ook Uptravi langer dan 3 achtereenvolgende dagen niet inneemt (als u achtereenvolgende doses heeft overgeslagen), neem dan onmiddellijk contact op met uw PAH-arts of -verpleegkundige omdat het nodig kan zijn uw dosis aan te passen om bijwerkingen te voorkomen. Uw arts of verpleegkundige kan u laten verdergaan met uw behandeling met een lagere dosis en deze dosis dan geleidelijk verhogen tot uw vorige onderhoudsdosis pp0.indd 9.. :3 Format/dimensions 0 x mm Page of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
22 Titratiedagboek 8 Lees de instructies in de bijsluiter aandachtig. De volgende dagboekpagina s helpen u om bij te houden hoeveel tabletten u s ochtends en s avonds tijdens de titratie moet innemen. Schrijf op deze pagina s op hoeveel tabletten u s ochtends en s avonds inneemt. Elke stap duurt meestal ongeveer week, tenzij uw arts of verpleegkundige u anders voorschrijft. Als uw titratiestappen langer duren dan week, zijn er extra dagboekpagina s om dit bij te houden. Gebruik de pagina s 20 tot en met 2 om de eerste weken van de behandeling bij te houden, wanneer u alleen tabletten van inneemt (stappen - 4). Als u tabletten van zowel als 800 voorgeschreven heeft gekregen, gebruik dan de pagina s 30 tot en met 3 (stappen - 8) pp0.indd :3 Format/dimensions 0 x mm Page 8 of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
23 Denk eraan dat u regelmatig uw PAH-arts of -verpleegkundige moet spreken. 9 Noteer hier de instructies van uw arts of verpleegkundige: Telefoonnummer van de praktijk van de arts en adres: Telefoonnummer van de apotheker: Aantekeningen: pp0.indd :3 Format/dimensions 0 x mm Page 9 of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
24 WEEK NR. Noteer elke dag in de vakjes hieronder hoeveel tabletten u s ochtends en s avonds neemt. Ik sprak met mijn arts of verpleegkundige op DD/MM/RR. Datum: 20 Avond Ochtend 0 De eerste inname van Uptravi moet s avonds zijn pp0.indd :3 Format/dimensions 0 x mm Page 20 of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
25 WEEK NR. Noteer het nummer van de week van de behandeling in de linkerbovenhoek. Noteer elke dag in de vakjes hieronder hoeveel tabletten u s ochtends en s avonds neemt. Ik sprak met mijn arts of verpleegkundige op DD/MM/RR. Datum: 2 Avond Ochtend De eerste inname van een verhoogde dosis Uptravi moet s avonds zijn pp0.indd :3 Format/dimensions 0 x mm Page 2 of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
26 WEEK NR. Noteer het nummer van de week van de behandeling in de linkerbovenhoek. Noteer elke dag in de vakjes hieronder hoeveel tabletten u s ochtends en s avonds neemt. Ik sprak met mijn arts of verpleegkundige op DD/MM/RR. Datum: 22 Avond Ochtend pp0.indd :3 Format/dimensions 0 x mm Page 22 of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
27 WEEK NR. Noteer het nummer van de week van de behandeling in de linkerbovenhoek. Noteer elke dag in de vakjes hieronder hoeveel tabletten u s ochtends en s avonds neemt. Ik sprak met mijn arts of verpleegkundige op DD/MM/RR. Datum: 23 Avond Ochtend Ga direct naar pagina 28 als uw arts tabletten van 800 voorschrijft pp0.indd :3 Format/dimensions 0 x mm Page 23 of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
28 WEEK NR. Noteer het nummer van de week van de behandeling in de linkerbovenhoek. Noteer elke dag in de vakjes hieronder hoeveel tabletten u s ochtends en s avonds neemt. Ik sprak met mijn arts of verpleegkundige op DD/MM/RR. Datum: 24 Avond Ochtend Ga direct naar pagina 28 als uw arts tabletten van 800 voorschrijft pp0.indd :3 Format/dimensions 0 x mm Page 24 of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
29 WEEK NR. Noteer het nummer van de week van de behandeling in de linkerbovenhoek. Noteer elke dag in de vakjes hieronder hoeveel tabletten u s ochtends en s avonds neemt. Ik sprak met mijn arts of verpleegkundige op DD/MM/RR. Datum: 2 Avond Ochtend Ga direct naar pagina 28 als uw arts tabletten van 800 voorschrijft pp0.indd :3 Format/dimensions 0 x mm Page 2 of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
30 WEEK NR. Noteer het nummer van de week van de behandeling in de linkerbovenhoek. Noteer elke dag in de vakjes hieronder hoeveel tabletten u s ochtends en s avonds neemt. Ik sprak met mijn arts of verpleegkundige op DD/MM/RR. Datum: 2 Avond Ochtend Ga direct naar pagina 28 als uw arts tabletten van 800 voorschrijft pp0.indd :3 Format/dimensions 0 x mm Page 2 of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
31 WEEK NR. Noteer het nummer van de week van de behandeling in de linkerbovenhoek. Noteer elke dag in de vakjes hieronder hoeveel tabletten u s ochtends en s avonds neemt. Ik sprak met mijn arts of verpleegkundige op DD/MM/RR. Datum: 2 Avond Ochtend Ga direct naar pagina 28 als uw arts tabletten van 800 voorschrijft pp0.indd :3 Format/dimensions 0 x mm Page 2 of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
32 28 tablet van tablet van 800 (Gebruiken bij stap tot en met 8 om het aantal benodigde tabletten per dosis te verminderen.) Gebruik de volgende dagboekpagina s als uw arts of verpleegkundige u niet alleen tabletten van, maar ook van 800 voorschrijft. Kruis elke dag op de dagboekpagina s aan dat u één tablet van 800 s ochtends en het voorgeschreven aantal tabletten van s avonds heeft ingenomen pp0.indd :3 Format/dimensions 0 x mm Page 28 of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
33 Denk eraan dat u regelmatig uw PAH-arts of -verpleegkundige moet spreken. 29 Noteer hier de instructies van uw arts of verpleegkundige: Telefoonnummer van de praktijk van de arts en adres: Telefoonnummer van de apotheker: Aantekeningen: pp0.indd :3 Format/dimensions 0 x mm Page 29 of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
34 WEEK NR. Noteer het nummer van de week van de behandeling in de linkerbovenhoek. Noteer elke dag in de vakjes hieronder hoeveel tabletten u s ochtends en s avonds neemt. Ik sprak met mijn arts of verpleegkundige op DD/MM/RR. Datum: 30 Avond Ochtend pp0.indd :3 Format/dimensions 0 x mm Page 30 of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
35 WEEK NR. Noteer het nummer van de week van de behandeling in de linkerbovenhoek. Noteer elke dag in de vakjes hieronder hoeveel tabletten u s ochtends en s avonds neemt. Ik sprak met mijn arts of verpleegkundige op DD/MM/RR. Datum: 3 Avond Ochtend pp0.indd :4 Format/dimensions 0 x mm Page 3 of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
36 WEEK NR. Noteer het nummer van de week van de behandeling in de linkerbovenhoek. Noteer elke dag in de vakjes hieronder hoeveel tabletten u s ochtends en s avonds neemt. Ik sprak met mijn arts of verpleegkundige op DD/MM/RR. Datum: 32 Avond Ochtend pp0.indd :4 Format/dimensions 0 x mm Page 32 of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
37 WEEK NR. Noteer het nummer van de week van de behandeling in de linkerbovenhoek. Noteer elke dag in de vakjes hieronder hoeveel tabletten u s ochtends en s avonds neemt. Ik sprak met mijn arts of verpleegkundige op DD/MM/RR. Datum: 33 Avond Ochtend pp0.indd :4 Format/dimensions 0 x mm Page 33 of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
38 WEEK NR. Noteer het nummer van de week van de behandeling in de linkerbovenhoek. Noteer elke dag in de vakjes hieronder hoeveel tabletten u s ochtends en s avonds neemt. Ik sprak met mijn arts of verpleegkundige op DD/MM/RR. Datum: 34 Avond Ochtend pp0.indd :4 Format/dimensions 0 x mm Page 34 of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
39 WEEK NR. Noteer het nummer van de week van de behandeling in de linkerbovenhoek. Noteer elke dag in de vakjes hieronder hoeveel tabletten u s ochtends en s avonds neemt. Ik sprak met mijn arts of verpleegkundige op DD/MM/RR. Datum: 3 Avond Ochtend pp0.indd :4 Format/dimensions 0 x mm Page 3 of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
40 WEEK NR. Noteer het nummer van de week van de behandeling in de linkerbovenhoek. Noteer elke dag in de vakjes hieronder hoeveel tabletten u s ochtends en s avonds neemt. Ik sprak met mijn arts of verpleegkundige op DD/MM/RR. Datum: 3 Avond Ochtend pp0.indd :4 Format/dimensions 0 x mm Page 3 of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
41 WEEK NR. Noteer het nummer van de week van de behandeling in de linkerbovenhoek. Noteer elke dag in de vakjes hieronder hoeveel tabletten u s ochtends en s avonds neemt. Ik sprak met mijn arts of verpleegkundige op DD/MM/RR. Datum: 3 Avond Ochtend pp0.indd :4 Format/dimensions 0 x mm Page 3 of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
42 Aantekeningen pp0.indd :4 Format/dimensions 0 x mm Page 38 of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
43 pp0.indd :4 Format/dimensions 0 x mm Page 39 of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
44 pp0.indd :4 Format/dimensions 0 x mm Page 40 of 40 4 Code no. SEM festgestellt werden, übernimmt die keine Haftung.! PLEASE TURN OVERPRINTING ON!
Titratiegids voor patiënten
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan hetin de handel brengen van het geneesmiddel Uptravi. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan hetin de handel brengen van het geneesmiddel Uptravi. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Bijsluiter: informatie voor de patiënt
 Bijsluiter: informatie voor de patiënt Uptravi 200 microgram filmomhulde tabletten Uptravi 400 microgram filmomhulde tabletten Uptravi 600 microgram filmomhulde tabletten Uptravi 800 microgram filmomhulde
Bijsluiter: informatie voor de patiënt Uptravi 200 microgram filmomhulde tabletten Uptravi 400 microgram filmomhulde tabletten Uptravi 600 microgram filmomhulde tabletten Uptravi 800 microgram filmomhulde
Risico-minimalisatiematerialen betreffende Farydak (panobinostat) voor patiënten
 r. H.G.J. Hoedemaker Medisch irecteur Oncology Novartis Pharma B.V. Raapopseweg 1 Postbus 241 NL - 6800 LZ ARNHEM Tel (+31) (0) 26 37 82 497 ax (+31) (0) 26 37 82 486 E-mail eric.hoedemaker@novartis.com
r. H.G.J. Hoedemaker Medisch irecteur Oncology Novartis Pharma B.V. Raapopseweg 1 Postbus 241 NL - 6800 LZ ARNHEM Tel (+31) (0) 26 37 82 497 ax (+31) (0) 26 37 82 486 E-mail eric.hoedemaker@novartis.com
Lees ook de volledige bijsluiter die u aantreft in de verpakking van dit geneesmiddel.
 Patiëntenbrochure met adviezen voor inname van Exjade (deferasirox) voor patiënten met bloedtransfusie-afhankelijke aandoeningen en chronische ijzerstapeling Lees ook de volledige bijsluiter die u aantreft
Patiëntenbrochure met adviezen voor inname van Exjade (deferasirox) voor patiënten met bloedtransfusie-afhankelijke aandoeningen en chronische ijzerstapeling Lees ook de volledige bijsluiter die u aantreft
Belangrijke Veiligheidsinformatie over prasugrel
 Belangrijke Veiligheidsinformatie over prasugrel Prasugrel behoort tot de farmacotherapeutische groep van de bloedplaatjesaggregatieremmers (heparine niet meegerekend), een groep waaronder ook clopidogrel
Belangrijke Veiligheidsinformatie over prasugrel Prasugrel behoort tot de farmacotherapeutische groep van de bloedplaatjesaggregatieremmers (heparine niet meegerekend), een groep waaronder ook clopidogrel
RISICO MINIMALISATIE MATERIAAL BETREFFENDE BARICITINIB VOOR DE VOORSCHRIJVER, APOTHEKER EN VERPLEEGKUNDIGE
 RISICO MINIMALISATIE MATERIAAL BETREFFENDE BARICITINIB VOOR DE VOORSCHRIJVER, APOTHEKER EN VERPLEEGKUNDIGE De risico minimalisatie materialen voor baricitinib zijn beoordeeld door het College ter Beoordeling
RISICO MINIMALISATIE MATERIAAL BETREFFENDE BARICITINIB VOOR DE VOORSCHRIJVER, APOTHEKER EN VERPLEEGKUNDIGE De risico minimalisatie materialen voor baricitinib zijn beoordeeld door het College ter Beoordeling
Voorlichtingsbrochure voor patiënten
 tolvaptan Voorlichtingsbrochure voor patiënten Additioneel risicominimalisatie-materiaal betreffende tolvaptan voor patiënten Samenvatting van risico s en risicobeperkende maatregelen. Het gebruik van
tolvaptan Voorlichtingsbrochure voor patiënten Additioneel risicominimalisatie-materiaal betreffende tolvaptan voor patiënten Samenvatting van risico s en risicobeperkende maatregelen. Het gebruik van
Risicominimalisatie-materiaal over de risico s van atomoxetine voor zorgverleners
 Risicominimalisatie-materiaal over de risico s van atomoxetine voor zorgverleners Atomoxetine 2/6 RISICOMINIMALISATIE-MATERIAAL OVER DE RISICO S VAN ATOMOXETINE VOOR ZORGVERLENERS Dit materiaal beschrijft
Risicominimalisatie-materiaal over de risico s van atomoxetine voor zorgverleners Atomoxetine 2/6 RISICOMINIMALISATIE-MATERIAAL OVER DE RISICO S VAN ATOMOXETINE VOOR ZORGVERLENERS Dit materiaal beschrijft
RISICO MINIMALISATIE MATERIAAL BETREFFENDE BARICITINIB VOOR DE VOORSCHRIJVER, APOTHEKER EN VERPLEEGKUNDIGE
 RISICO MINIMALISATIE MATERIAAL BETREFFENDE BARICITINIB VOOR DE VOORSCHRIJVER, APOTHEKER EN VERPLEEGKUNDIGE De risico minimalisatie materialen voor baricitinib zijn beoordeeld door het College ter Beoordeling
RISICO MINIMALISATIE MATERIAAL BETREFFENDE BARICITINIB VOOR DE VOORSCHRIJVER, APOTHEKER EN VERPLEEGKUNDIGE De risico minimalisatie materialen voor baricitinib zijn beoordeeld door het College ter Beoordeling
Risicominimalisatiemateriaal betreffende Valdoxan (agomelatine) voor zorgverleners:
 Risicominimalisatiemateriaal betreffende Valdoxan (agomelatine) voor zorgverleners: hernieuwde aandacht t.b.v. aanbevelingen voor monitoring van de leverfunctie Valdoxan en het risico op levertoxiciteit
Risicominimalisatiemateriaal betreffende Valdoxan (agomelatine) voor zorgverleners: hernieuwde aandacht t.b.v. aanbevelingen voor monitoring van de leverfunctie Valdoxan en het risico op levertoxiciteit
Risico minimalisatie materiaal betreffende Aripiprazol Sandoz (aripiprazol)
 Risico minimalisatie materiaal betreffende Aripiprazol Sandoz (aripiprazol) Dit risico materiaal is beoordeeld door het College ter Beoordeling van Geneesmiddelen (CBG) en beschrijft aanbevelingen voor
Risico minimalisatie materiaal betreffende Aripiprazol Sandoz (aripiprazol) Dit risico materiaal is beoordeeld door het College ter Beoordeling van Geneesmiddelen (CBG) en beschrijft aanbevelingen voor
Leidraad voor artsen voor het beoordelen en monitoren van cardiovasculaire risico bij het voorschrijven van atomoxetine
 Leidraad voor artsen voor het beoordelen en monitoren van cardiovasculaire risico bij het voorschrijven van atomoxetine Dit materiaal beschrijft aanbevelingen om belangrijke risico s van atomoxetine te
Leidraad voor artsen voor het beoordelen en monitoren van cardiovasculaire risico bij het voorschrijven van atomoxetine Dit materiaal beschrijft aanbevelingen om belangrijke risico s van atomoxetine te
(vandetanib) Dit geneesmiddel is onderworpen aan aanvullende monitoring.
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Caprelsa. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Caprelsa. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Risico Minimalisatie Materiaal. betreffende tolcapon 100 mg en 200 mg tabletten. voor patiënten
 Risico Minimalisatie Materiaal betreffende tolcapon 100 mg en 200 mg tabletten voor patiënten Inleiding Dit dagboek beschrijft aanbevelingen om belangrijke risico s van het geneesmiddel te beperken of
Risico Minimalisatie Materiaal betreffende tolcapon 100 mg en 200 mg tabletten voor patiënten Inleiding Dit dagboek beschrijft aanbevelingen om belangrijke risico s van het geneesmiddel te beperken of
Datum. Patiënten dienen in staat te zijn zich te houden aan de vereisten voor het veilig gebruik van macitentan.
 1/2 Betreft: Risicominimalisatie-materialen betreffende macitentan voor voorschrijvers Datum Geachte heer/mevrouw, In overleg met het College ter Beoordeling van Geneesmiddelen willen wij u graag informeren
1/2 Betreft: Risicominimalisatie-materialen betreffende macitentan voor voorschrijvers Datum Geachte heer/mevrouw, In overleg met het College ter Beoordeling van Geneesmiddelen willen wij u graag informeren
PRAKTISCHE PATIËNTENINFORMATIE
 PRAKTISCHE PATIËNTENINFORMATIE STARTEN MET ISENTRESS Samen met uw arts heeft u besloten ISENTRESS (raltegravir, MSD) als één van de HIVgeneesmiddelen te gaan gebruiken voor de behandeling van HIV. In
PRAKTISCHE PATIËNTENINFORMATIE STARTEN MET ISENTRESS Samen met uw arts heeft u besloten ISENTRESS (raltegravir, MSD) als één van de HIVgeneesmiddelen te gaan gebruiken voor de behandeling van HIV. In
! BELANGRIJKE INFORMATIE
 ! BELANGRIJKE INFORMATIE Belangrijke informatie over emtricitabine/tenofovirdisoproxil 200 mg/245mg filmomhulde tabletten als PrEP om het risico op het krijgen van een infectie met het humaan immunodeficiëntievirus
! BELANGRIJKE INFORMATIE Belangrijke informatie over emtricitabine/tenofovirdisoproxil 200 mg/245mg filmomhulde tabletten als PrEP om het risico op het krijgen van een infectie met het humaan immunodeficiëntievirus
<GEADRESSEERDE> <ADRES> <POSTCODE WOONPLAATS> <Datum> Ref.: lvd/015086
 Ref.: lvd/015086 Onderwerp: Risico minimalisatie materialen betreffende Toujeo voor zorgverleners en voor patiënten die omgezet worden van of naar
Ref.: lvd/015086 Onderwerp: Risico minimalisatie materialen betreffende Toujeo voor zorgverleners en voor patiënten die omgezet worden van of naar
Starten met Otezla, Psoriasis & artritis psoriatica. doet. zo doet u dat. Hoofdhuidpsoriasis. Vermoeidheid. Kwaliteit van leven.
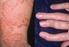 Psoriasis & artritis psoriatica Starten met Otezla, Vermoeidheid Kwaliteit van leven Worstenvingers en -tenen (dactylitis) Peesontsteking (enthesitis) zo doet u dat doet Hoofdhuidpsoriasis Jeuk Plaques
Psoriasis & artritis psoriatica Starten met Otezla, Vermoeidheid Kwaliteit van leven Worstenvingers en -tenen (dactylitis) Peesontsteking (enthesitis) zo doet u dat doet Hoofdhuidpsoriasis Jeuk Plaques
Samenvatting van risico s en acties om deze te voorkomen of verminderen:
 T.a.v. Adresregel 1 Adresregel 2 Risico minimalisatie materialen betreffende: BOTOX, botulinum toxine type A, voor artsen en patiënten. Geachte Heer / Mevrouw In overleg met het College ter Beoordeling
T.a.v. Adresregel 1 Adresregel 2 Risico minimalisatie materialen betreffende: BOTOX, botulinum toxine type A, voor artsen en patiënten. Geachte Heer / Mevrouw In overleg met het College ter Beoordeling
Voorlichtingsmateriaal betreffende sebelipase alfa voor de zorgverlener. Belangrijke veiligheidsinformatie
 Voorlichtingsmateriaal betreffende sebelipase alfa voor de zorgverlener Belangrijke veiligheidsinformatie Risico minimalisatie materiaal betreffende sebelipase alfa voor zorgverleners - versie 2-03/2018
Voorlichtingsmateriaal betreffende sebelipase alfa voor de zorgverlener Belangrijke veiligheidsinformatie Risico minimalisatie materiaal betreffende sebelipase alfa voor zorgverleners - versie 2-03/2018
Patiënten dienen in staat te zijn zich te houden aan de vereisten voor het veilig gebruik van macitentan.
 1/2 Betreft: Risicominimalisatie-materialen betreffende macitentan voor voorschrijvers dd - mm - jjjj Geachte heer / mevrouw, In overleg met het College ter Beoordeling van Geneesmiddelen willen wij u
1/2 Betreft: Risicominimalisatie-materialen betreffende macitentan voor voorschrijvers dd - mm - jjjj Geachte heer / mevrouw, In overleg met het College ter Beoordeling van Geneesmiddelen willen wij u
Richtlijn voor apothekers betreffende. Alofisel. (darvadstrocel) Ontvangst- en bewaringsinstructies. Versie
 Richtlijn voor apothekers betreffende Alofisel (darvadstrocel) Ontvangst- en bewaringsinstructies 1 De risico minimalisatie materialen voor darvadstrocel zijn beoordeeld door het College ter Beoordeling
Richtlijn voor apothekers betreffende Alofisel (darvadstrocel) Ontvangst- en bewaringsinstructies 1 De risico minimalisatie materialen voor darvadstrocel zijn beoordeeld door het College ter Beoordeling
Alphen aan den Rijn, november 2015
 Novo Nordisk B.V. Flemingweg 18 2408 AV Alphen aan den Rijn Nederland Postbus 443 2400 AK Alphen aan den Rijn Nederland Alphen aan den Rijn, november 2015 Ref: Lzvt/Elee/005 Betreft: Belangrijke veiligheidsinformatie
Novo Nordisk B.V. Flemingweg 18 2408 AV Alphen aan den Rijn Nederland Postbus 443 2400 AK Alphen aan den Rijn Nederland Alphen aan den Rijn, november 2015 Ref: Lzvt/Elee/005 Betreft: Belangrijke veiligheidsinformatie
Zepatier. Elbasvir + Grazoprevir Product Informatie Fiche. T +32(0) F +32(0) Campus Sint-Jan Schiepse bos 6
 Zepatier Elbasvir + Grazoprevir Product Informatie Fiche T +32(0)89 32 50 50 F +32(0)89 32 79 00 info@zol.be Campus Sint-Jan Schiepse bos 6 B 3600 Genk Campus Sint-Barbara Bessemerstraat 478 B 3620 Lanaken
Zepatier Elbasvir + Grazoprevir Product Informatie Fiche T +32(0)89 32 50 50 F +32(0)89 32 79 00 info@zol.be Campus Sint-Jan Schiepse bos 6 B 3600 Genk Campus Sint-Barbara Bessemerstraat 478 B 3620 Lanaken
Risicominimalisatie materiaal betreffende Exjade (deferasirox) voor patiënten met bloedtransfusie-afhankelijke aandoeningen en chronische
 Risicominimalisatie materiaal betreffende Exjade (deferasirox) voor patiënten met bloedtransfusie-afhankelijke aandoeningen en chronische ijzerstapeling 2 Risicominimalisatie materiaal betreffende Exjade
Risicominimalisatie materiaal betreffende Exjade (deferasirox) voor patiënten met bloedtransfusie-afhankelijke aandoeningen en chronische ijzerstapeling 2 Risicominimalisatie materiaal betreffende Exjade
Betreft: Risico minimalisatie materialen betreffende zoledroninezuur (een bisfosfonaat)
 Fresenius Kabi Nederland BV Amersfoortseweg 10E 3705 GJ Zeist [datum] Betreft: Risico minimalisatie materialen betreffende zoledroninezuur (een bisfosfonaat) Geachte Heer/Mevrouw, In overleg met het College
Fresenius Kabi Nederland BV Amersfoortseweg 10E 3705 GJ Zeist [datum] Betreft: Risico minimalisatie materialen betreffende zoledroninezuur (een bisfosfonaat) Geachte Heer/Mevrouw, In overleg met het College
Glucofleks 595 mg, filmomhulde tabletten glucosaminesulfaat kaliumchloride
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER Glucofleks 595 mg, filmomhulde tabletten glucosaminesulfaat kaliumchloride Lees de hele bijsluiter zorgvuldig door, want deze bevat belangrijke informatie voor
BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER Glucofleks 595 mg, filmomhulde tabletten glucosaminesulfaat kaliumchloride Lees de hele bijsluiter zorgvuldig door, want deze bevat belangrijke informatie voor
Voorlichtingsmateriaal betreffende Kanuma (sebelipase alfa) voor de zorgverlener. Belangrijke veiligheidsinformatie
 Voorlichtingsmateriaal betreffende Kanuma (sebelipase alfa) voor de zorgverlener Belangrijke veiligheidsinformatie Risico minimalisatie materiaal KANUMA - versie 05/2016 De risico minimalisatie materialen
Voorlichtingsmateriaal betreffende Kanuma (sebelipase alfa) voor de zorgverlener Belangrijke veiligheidsinformatie Risico minimalisatie materiaal KANUMA - versie 05/2016 De risico minimalisatie materialen
Risicominimalisatie materiaal betreffende Actiq (fentanyl) Voor patiënten
 Risicominimalisatie materiaal betreffende Actiq (fentanyl) Voor patiënten Teva Nederland BV Swensweg 5 Postbus 552 2003 RN Haarlem 0800 02 28 400 Versie 1.0 Deze risico minimalisatie materialen voor Actiq
Risicominimalisatie materiaal betreffende Actiq (fentanyl) Voor patiënten Teva Nederland BV Swensweg 5 Postbus 552 2003 RN Haarlem 0800 02 28 400 Versie 1.0 Deze risico minimalisatie materialen voor Actiq
Informatie voor patiënt, ouders en/of verzorgers van de patiënt
 Informatie voor patiënt, ouders en/of verzorgers van de patiënt Versie 5, mei 2019 Let op bij gebruik van fingolimod. Fingolimod is het werkzaam bestanddeel in het medicijn. Uw medicijn kan ook een andere
Informatie voor patiënt, ouders en/of verzorgers van de patiënt Versie 5, mei 2019 Let op bij gebruik van fingolimod. Fingolimod is het werkzaam bestanddeel in het medicijn. Uw medicijn kan ook een andere
Risicominimalisatie materiaal voor patiënten betreffende mycofenolaat-bevattende geneesmiddelen
 Risicominimalisatie materiaal voor patiënten betreffende mycofenolaat-bevattende geneesmiddelen Dit risicominimalisatie materiaal voor mycofenolaat-bevattende geneesmiddelen is beoordeeld door het College
Risicominimalisatie materiaal voor patiënten betreffende mycofenolaat-bevattende geneesmiddelen Dit risicominimalisatie materiaal voor mycofenolaat-bevattende geneesmiddelen is beoordeeld door het College
Package Leaflet
 1.3.1.3 Package Leaflet 1.3.1.3-1 Bijsluiter: informatie voor de gebruiker Etos Hooikoortstabletten Loratadine 10 mg, tabletten loratadine Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken,
1.3.1.3 Package Leaflet 1.3.1.3-1 Bijsluiter: informatie voor de gebruiker Etos Hooikoortstabletten Loratadine 10 mg, tabletten loratadine Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken,
Belangrijke veiligheidsinformatie over dapagliflozine alleen voor diabetes type 1
 Belangrijke veiligheidsinformatie over dapagliflozine alleen voor diabetes type 1 Let op bij het gebruik van dapagliflozine. Dapagliflozine is het werkzame bestanddeel in het medicijn. Uw medicijn kan
Belangrijke veiligheidsinformatie over dapagliflozine alleen voor diabetes type 1 Let op bij het gebruik van dapagliflozine. Dapagliflozine is het werkzame bestanddeel in het medicijn. Uw medicijn kan
BELANGRIJKE VEILIGHEIDSINFORMATIE
 Aanbevelingen Neem de volledige medische voorgeschiedenis van de patiënt in overweging, inclusief enig eerder of gelijktijdig gebruikte biological BELANGRIJKE VEILIGHEIDSINFORMATIE Er is geen ervaring
Aanbevelingen Neem de volledige medische voorgeschiedenis van de patiënt in overweging, inclusief enig eerder of gelijktijdig gebruikte biological BELANGRIJKE VEILIGHEIDSINFORMATIE Er is geen ervaring
RIVASTIGMINE TEVA 4,6 MG/24 U, 9,5 MG/24 U,
 Nederland RIVASTIGMINE TEVA 4,6 MG/24 U, 9,5 MG/24 U, 13,3 mg/24 U, pleister voor transdermaal gebruik Gebruiksaanwijziging en Patiëntendagboek RVG 112335 RVG 112336 RVG 115219 Teva Nederland BV Swensweg
Nederland RIVASTIGMINE TEVA 4,6 MG/24 U, 9,5 MG/24 U, 13,3 mg/24 U, pleister voor transdermaal gebruik Gebruiksaanwijziging en Patiëntendagboek RVG 112335 RVG 112336 RVG 115219 Teva Nederland BV Swensweg
PATIËNTENBIJSLUITER. CRESTOR (rosuvastatine) Lees deze bijsluiter zorgvuldig door voordat u start met het gebruik van dit geneesmiddel.
 PATIËNTENBIJSLUITER CRESTOR (rosuvastatine) Lees deze bijsluiter zorgvuldig door voordat u start met het gebruik van dit geneesmiddel. Bewaar deze bijsluiter, het kan nodig zijn om deze nogmaals door te
PATIËNTENBIJSLUITER CRESTOR (rosuvastatine) Lees deze bijsluiter zorgvuldig door voordat u start met het gebruik van dit geneesmiddel. Bewaar deze bijsluiter, het kan nodig zijn om deze nogmaals door te
Prod. oktober 2014, NL/TRIM/0001/14, Exp. oktober 2016. Triumeq. Starten met. Patiënteninformatie
 Prod. oktober 2014, NL/TRIM/0001/14, Exp. oktober 2016 Starten met Triumeq Patiënteninformatie Vooraf U krijgt deze folder omdat u Triumeq gaat gebruiken om hiv te remmen. In deze folder vindt u de belangrijkste
Prod. oktober 2014, NL/TRIM/0001/14, Exp. oktober 2016 Starten met Triumeq Patiënteninformatie Vooraf U krijgt deze folder omdat u Triumeq gaat gebruiken om hiv te remmen. In deze folder vindt u de belangrijkste
Viekirax. Ombitasvir + Paritaprevir + Ritonavir Product Informatie Fiche. T +32(0) F +32(0)
 Viekirax Ombitasvir + Paritaprevir + Ritonavir Product Informatie Fiche T +32(0)89 32 50 50 F +32(0)89 32 79 00 info@zol.be Campus Sint-Jan Schiepse bos 6 B 3600 Genk Campus Sint-Barbara Bessemerstraat
Viekirax Ombitasvir + Paritaprevir + Ritonavir Product Informatie Fiche T +32(0)89 32 50 50 F +32(0)89 32 79 00 info@zol.be Campus Sint-Jan Schiepse bos 6 B 3600 Genk Campus Sint-Barbara Bessemerstraat
RVG 23266/ Version 2014_01 Page 1 of 5 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER
 Version 2014_01 Page 1 of 5 1.3.1.3 PATIENT INFORMATION LEAFLET BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER BETAHISTINE dihcl APOTEX 8 MG, TABLETTEN BETAHISTINE dihcl APOTEX 16 MG, TABLETTEN Betahistine dihydrochloride
Version 2014_01 Page 1 of 5 1.3.1.3 PATIENT INFORMATION LEAFLET BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER BETAHISTINE dihcl APOTEX 8 MG, TABLETTEN BETAHISTINE dihcl APOTEX 16 MG, TABLETTEN Betahistine dihydrochloride
Patiënten informatiegids voor behandeling met Effentora
 Patiënten informatiegids voor behandeling met Effentora Informatie in het kader van het Effentora Risk Management Plan Teva Nederland BV Swensweg 5 Postbus 552 2003 RN Haarlem 0800 02 28 400 Effentora
Patiënten informatiegids voor behandeling met Effentora Informatie in het kader van het Effentora Risk Management Plan Teva Nederland BV Swensweg 5 Postbus 552 2003 RN Haarlem 0800 02 28 400 Effentora
Emtricitabine/Tenofovirdisoproxil Krka 200 mg/245 mg filmomhulde tabletten (emtricitabine/tenofovirdisoproxil)
 Om een maximaal voordeel te halen voor uw gezondheid uit de effecten van het geneesmiddel Emtricitabine/Tenofovirdisoproxil Krka 200 mg/245 mg filmomhulde tabletten, om voor een goed gebruik ervan te zorgen
Om een maximaal voordeel te halen voor uw gezondheid uit de effecten van het geneesmiddel Emtricitabine/Tenofovirdisoproxil Krka 200 mg/245 mg filmomhulde tabletten, om voor een goed gebruik ervan te zorgen
Bijlage III. Wijzigingen die moeten worden aangebracht in de desbetreffende rubrieken van de Samenvatting van de Productkenmerken en de Bijsluiters
 Bijlage III Wijzigingen die moeten worden aangebracht in de desbetreffende rubrieken van de Samenvatting van de Productkenmerken en de Bijsluiters NB: Deze Samenvatting van de productkenmerken, Etikettering
Bijlage III Wijzigingen die moeten worden aangebracht in de desbetreffende rubrieken van de Samenvatting van de Productkenmerken en de Bijsluiters NB: Deze Samenvatting van de productkenmerken, Etikettering
Breda, 25 juni 2018 Ref.: PHNL/HIV/0618/0006
 Breda, 25 juni 2018 Ref.: PHNL/HIV/0618/0006 Belangrijke risico-informatie: Verhoogd risico op falen van de behandeling en verhoogd risico op transmissie van de hiv-infectie van moeder op kind door lage
Breda, 25 juni 2018 Ref.: PHNL/HIV/0618/0006 Belangrijke risico-informatie: Verhoogd risico op falen van de behandeling en verhoogd risico op transmissie van de hiv-infectie van moeder op kind door lage
HANDLEIDING VOOR DE VOORSCHRIJVER
 HANDLEIDING VOOR DE VOORSCHRIJVER Handleiding voor de voorschrijver CERDELGA is geïndiceerd voor de langetermijnbehandeling van volwassen patiënten met de ziekte van Gaucher type 1. Deze handleiding is
HANDLEIDING VOOR DE VOORSCHRIJVER Handleiding voor de voorschrijver CERDELGA is geïndiceerd voor de langetermijnbehandeling van volwassen patiënten met de ziekte van Gaucher type 1. Deze handleiding is
Dancor 10, tabletten 10 mg Dancor 20, tabletten 20 mg
 DANCOR 10/20 bijsluiter 31-01-2008 blz. 1 / 5 Lees deze bijsluiter zorgvuldig door voordat u start met het gebruik van dit geneesmiddel. Bewaar deze bijsluiter, het kan nodig zijn om deze nogmaals door
DANCOR 10/20 bijsluiter 31-01-2008 blz. 1 / 5 Lees deze bijsluiter zorgvuldig door voordat u start met het gebruik van dit geneesmiddel. Bewaar deze bijsluiter, het kan nodig zijn om deze nogmaals door
Begeleiding bij het gebruik van medicijnen bij dementie
 Uw geriater heeft u het medicijn galantamine, rivastigmine (pillen of pleisters), memantine of donepezil voorgeschreven. In het MCL begeleiden wij u en uw mantelzorger bij het gebruik van deze medicijnen.
Uw geriater heeft u het medicijn galantamine, rivastigmine (pillen of pleisters), memantine of donepezil voorgeschreven. In het MCL begeleiden wij u en uw mantelzorger bij het gebruik van deze medicijnen.
Prod. Maart 2014, NL/DLG/0022/14, Exp. Maart Tivicay. Starten met. Patiënteninformatie
 Prod. Maart 2014, NL/DLG/0022/14, Exp. Maart 2014 Starten met Tivicay Patiënteninformatie Vooraf U krijgt deze folder omdat u Tivicay en andere medicijnen gaat gebruiken om hiv te remmen. In deze folder
Prod. Maart 2014, NL/DLG/0022/14, Exp. Maart 2014 Starten met Tivicay Patiënteninformatie Vooraf U krijgt deze folder omdat u Tivicay en andere medicijnen gaat gebruiken om hiv te remmen. In deze folder
10 tips voor een veilig geneesmiddelengebruik. 18 november 2013 az Sint-Blasius Dendermonde Meer info? info@azsintblasius.be
 10 tips voor een veilig geneesmiddelengebruik 18 november 2013 az Sint-Blasius Dendermonde Meer info? info@azsintblasius.be Als je ziek bent of ouder wordt moet je vaak verschillende geneesmiddelen innemen.
10 tips voor een veilig geneesmiddelengebruik 18 november 2013 az Sint-Blasius Dendermonde Meer info? info@azsintblasius.be Als je ziek bent of ouder wordt moet je vaak verschillende geneesmiddelen innemen.
Risico minimalisatie materiaal betreffende. voor patiënten
 Risico minimalisatie materiaal betreffende lomitapide voor patiënten De risico minimalisatie materialen voor lomitapide zijn beoordeeld door het College ter Beoordeling van Geneesmiddelen (CBG). Deze materialen
Risico minimalisatie materiaal betreffende lomitapide voor patiënten De risico minimalisatie materialen voor lomitapide zijn beoordeeld door het College ter Beoordeling van Geneesmiddelen (CBG). Deze materialen
Cytomel 25 microgram, tabletten Cytomel 12,5 microgram, tabletten Cytomel 5 microgram, tabletten
 BIJSLUITER: INFORMATIE VOOR GEBRUIKERS Cytomel 25 microgram, tabletten Cytomel 12,5 microgram, tabletten Cytomel 5 microgram, tabletten Liothyronine (in de vorm van liothyroninenatrium) Lees goed de hele
BIJSLUITER: INFORMATIE VOOR GEBRUIKERS Cytomel 25 microgram, tabletten Cytomel 12,5 microgram, tabletten Cytomel 5 microgram, tabletten Liothyronine (in de vorm van liothyroninenatrium) Lees goed de hele
Servicepunt van de Hiv Vereniging Nederland Tel. 020-689 2577 Bereikbaar van maandag t/m vrijdag, tussen 14.00 en 22.00 uur
 Nuttige adressen: Servicepunt van de Hiv Vereniging Nederland Tel. 020-689 2577 Bereikbaar van maandag t/m vrijdag, tussen 14.00 en 22.00 uur Aids SOA infolijn Tel. 0900-204 2040 (10 eurocent per minuut)
Nuttige adressen: Servicepunt van de Hiv Vereniging Nederland Tel. 020-689 2577 Bereikbaar van maandag t/m vrijdag, tussen 14.00 en 22.00 uur Aids SOA infolijn Tel. 0900-204 2040 (10 eurocent per minuut)
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER. Paracetamol Mylan 500 mg tabletten Paracetamol
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Paracetamol Mylan 500 mg tabletten Paracetamol Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie in voor
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Paracetamol Mylan 500 mg tabletten Paracetamol Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie in voor
Dagboekje voor de opvolging van uw behandeling
 Dagboekje voor de opvolging van uw behandeling Dit boekje behoort toe aan Beste patiënt(e), Uw arts heeft u een geneesmiddel voorgeschreven ter behandeling van melanoom, een specifieke vorm van huidkanker.
Dagboekje voor de opvolging van uw behandeling Dit boekje behoort toe aan Beste patiënt(e), Uw arts heeft u een geneesmiddel voorgeschreven ter behandeling van melanoom, een specifieke vorm van huidkanker.
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER. fexofenadinehydrochloride
 Sandoz B.V. Page 1/5 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Fexofenadine Sandoz 120 mg, filmomhulde tabletten fexofenadinehydrochloride Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken
Sandoz B.V. Page 1/5 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Fexofenadine Sandoz 120 mg, filmomhulde tabletten fexofenadinehydrochloride Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken
Risicominimalisatie-materiaal over de risico s van dapagliflozine alleen voor diabetes mellitus type 1
 Risicominimalisatie-materiaal over de risico s van dapagliflozine alleen voor diabetes mellitus type 1 Brochure voor zorgverleners om het risico op diabetische ketoacidose (DKA) bij het gebruik van dapagliflozine
Risicominimalisatie-materiaal over de risico s van dapagliflozine alleen voor diabetes mellitus type 1 Brochure voor zorgverleners om het risico op diabetische ketoacidose (DKA) bij het gebruik van dapagliflozine
Directe communicatie aan gezondheidszorgbeoefenaars over de associatie van Sprycel (dasatinib) met Pulmonaire Arteriële Hypertensie (PAH)
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Belangrijke aandachtspunten
 1.8.2 armm Rev.nr. 1711 Pag. 1 van Risicominimalisatiemateriaal voor voorschrijvers Brochure controle nierfunctie bij behandeling van volwassenen met chronische hepatitis B De risico minimalisatie materialen
1.8.2 armm Rev.nr. 1711 Pag. 1 van Risicominimalisatiemateriaal voor voorschrijvers Brochure controle nierfunctie bij behandeling van volwassenen met chronische hepatitis B De risico minimalisatie materialen
Isosorbidedinitraat 5 PCH, tabletten voor oromucosaal gebruik 5 mg isosorbidedinitraat
 1.3.1 : Bijsluiter Bladzijde : 1 BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER Isosorbidedinitraat 5 PCH, 5 mg isosorbidedinitraat Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken,
1.3.1 : Bijsluiter Bladzijde : 1 BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER Isosorbidedinitraat 5 PCH, 5 mg isosorbidedinitraat Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken,
Betahistine dihcl 8 mg Teva, tabletten Betahistine dihcl 16 mg Teva, tabletten betahistinedihydrochloride
 1.3.1 : Bijsluiter Bladzijde : 1 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Betahistine dihcl 8 mg Teva, Betahistine dihcl 16 mg Teva, betahistinedihydrochloride Lees goed de hele bijsluiter voordat u dit
1.3.1 : Bijsluiter Bladzijde : 1 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Betahistine dihcl 8 mg Teva, Betahistine dihcl 16 mg Teva, betahistinedihydrochloride Lees goed de hele bijsluiter voordat u dit
BIJSLUITER. SPIRONOLACTON 12,5 mg tablet
 BIJSLUITER SPIRONOLACTON 12,5 mg tablet Lees de hele bijsluiter goed voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie in voor u. - Bewaar deze bijsluiter. Misschien heeft
BIJSLUITER SPIRONOLACTON 12,5 mg tablet Lees de hele bijsluiter goed voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie in voor u. - Bewaar deze bijsluiter. Misschien heeft
Risico-minimalisatiemateriaal betreffende Tasigna (nilotinib) voor voorschrijvers en apothekers
 Risico-minimalisatiemateriaal betreffende Tasigna (nilotinib) voor voorschrijvers en apothekers Introductie De risico-minimalisatiematerialen voor Tasigna (nilotinib) zijn beoordeeld door het College ter
Risico-minimalisatiemateriaal betreffende Tasigna (nilotinib) voor voorschrijvers en apothekers Introductie De risico-minimalisatiematerialen voor Tasigna (nilotinib) zijn beoordeeld door het College ter
Mekinist Trametinib. Product Informatie Fiche. T +32(0) F +32(0) Campus Sint-Jan Schiepse bos 6.
 Mekinist Trametinib Product Informatie Fiche T +32(0)89 32 50 50 F +32(0)89 32 79 00 info@zol.be Campus Sint-Jan Schiepse bos 6 B 3600 Genk Campus Sint-Barbara Bessemerstraat 478 B 3620 Lanaken Medisch
Mekinist Trametinib Product Informatie Fiche T +32(0)89 32 50 50 F +32(0)89 32 79 00 info@zol.be Campus Sint-Jan Schiepse bos 6 B 3600 Genk Campus Sint-Barbara Bessemerstraat 478 B 3620 Lanaken Medisch
Lactulose EG 670 mg/ml, siroop Lactulose EG 670 mg/ml, siroop in zakjes Lactulose EG 10 g, poeder voor drank (zakjes)
 BIJSLUITER Lees de hele bijsluiter aandachtig door, omdat er voor u belangrijke informatie in staat. Dit geneesmiddel is zonder voorschrift verkrijgbaar. Desalniettemin dient u lactulose zorgvuldig te
BIJSLUITER Lees de hele bijsluiter aandachtig door, omdat er voor u belangrijke informatie in staat. Dit geneesmiddel is zonder voorschrift verkrijgbaar. Desalniettemin dient u lactulose zorgvuldig te
BIJSLUITER. Inhoud van deze bijsluiter
 BIJSLUITER Lees de hele bijsluiter aandachtig door alvorens dit geneesmiddel in te nemen Bewaar deze bijsluiter, misschien heeft u hem nog een keer nodig. Raadpleeg uw arts of apotheker, als u aanvullende
BIJSLUITER Lees de hele bijsluiter aandachtig door alvorens dit geneesmiddel in te nemen Bewaar deze bijsluiter, misschien heeft u hem nog een keer nodig. Raadpleeg uw arts of apotheker, als u aanvullende
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER. Riluzol SUN 50 mg filmomhulde tabletten Riluzol
 BIJSLUITER 1 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Riluzol SUN 50 mg filmomhulde tabletten Riluzol Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie
BIJSLUITER 1 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Riluzol SUN 50 mg filmomhulde tabletten Riluzol Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER. Lactulose EG 670 mg/ml, siroop Lactulose EG 10 g, poeder voor drank. lactulose
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Lactulose EG 10 g, poeder voor drank lactulose Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie in voor
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Lactulose EG 10 g, poeder voor drank lactulose Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie in voor
BIJSLUITER. Inhoud van deze bijsluiter:
 BIJSLUITER Lees de hele bijsluiter aandachtig door, omdat er voor u belangrijke informatie in staat. Raadpleeg uw arts of apotheker als u aanvullende vragen heeft. Bewaar deze bijsluiter, misschien heeft
BIJSLUITER Lees de hele bijsluiter aandachtig door, omdat er voor u belangrijke informatie in staat. Raadpleeg uw arts of apotheker als u aanvullende vragen heeft. Bewaar deze bijsluiter, misschien heeft
Risico minimalisatie materialen betreffende Inflectra (infliximab) voor de voorschrijvers
 Inflectra (infliximab) Dit geneesmiddel is onderworpen aan aanvullende monitoring Risico minimalisatie materialen betreffende Inflectra (infliximab) voor de voorschrijvers De risico minimalisatie materialen
Inflectra (infliximab) Dit geneesmiddel is onderworpen aan aanvullende monitoring Risico minimalisatie materialen betreffende Inflectra (infliximab) voor de voorschrijvers De risico minimalisatie materialen
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER. Betaserc, tabletten 8 of 16 mg. Betahistine dihydrochloride
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Betaserc, tabletten 8 of 16 mg Betahistine dihydrochloride Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken, want er staat belangrijke informatie
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Betaserc, tabletten 8 of 16 mg Betahistine dihydrochloride Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken, want er staat belangrijke informatie
CRIZOTINIB (XALKORI )
 CRIZOTINIB (XALKORI ) KANKERCENTRUM Onco_thor_019 INHOUDSOPGAVE 01 Wat doet dit geneesmiddel? 3 02 Inname 3 03 Pletten / breken 3 04 Combinatie met andere geneesmiddelen 4 05 Bijzondere voorzorgsmaatregelen
CRIZOTINIB (XALKORI ) KANKERCENTRUM Onco_thor_019 INHOUDSOPGAVE 01 Wat doet dit geneesmiddel? 3 02 Inname 3 03 Pletten / breken 3 04 Combinatie met andere geneesmiddelen 4 05 Bijzondere voorzorgsmaatregelen
Package Leaflet
 1.3.1.3 Package Leaflet 1.3.1.3-1 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Etos Hooikoortstabletten Loratadine 10 mg, tabletten loratadine Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken,
1.3.1.3 Package Leaflet 1.3.1.3-1 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Etos Hooikoortstabletten Loratadine 10 mg, tabletten loratadine Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken,
Glivec - Imatinib. Product Informatie Fiche. T +32(0) F +32(0) Campus Sint-Jan Schiepse bos 6.
 Glivec - Imatinib Product Informatie Fiche T +32(0)89 32 50 50 F +32(0)89 32 79 00 info@zol.be Campus Sint-Jan Schiepse bos 6 B 3600 Genk Campus Sint-Barbara Bessemerstraat 478 B 3620 Lanaken Medisch Centrum
Glivec - Imatinib Product Informatie Fiche T +32(0)89 32 50 50 F +32(0)89 32 79 00 info@zol.be Campus Sint-Jan Schiepse bos 6 B 3600 Genk Campus Sint-Barbara Bessemerstraat 478 B 3620 Lanaken Medisch Centrum
Package leaflet / 1 van 6
 1.3.1.3 Package leaflet 1.3.1.3 / 1 van 6 Bijsluiter: informatie voor de gebruiker Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken, want er staat belangrijke informatie in voor u.
1.3.1.3 Package leaflet 1.3.1.3 / 1 van 6 Bijsluiter: informatie voor de gebruiker Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken, want er staat belangrijke informatie in voor u.
Rhinofebryl, harde capsules
 Pagina 1 van 6 Lees de hele bijsluiter aandachtig door, omdat er voor u belangrijke informatie in staat. Dit geneesmiddel is zonder voorschrift verkrijgbaar. Desalniettemin dient u "Rhinofebryl, harde
Pagina 1 van 6 Lees de hele bijsluiter aandachtig door, omdat er voor u belangrijke informatie in staat. Dit geneesmiddel is zonder voorschrift verkrijgbaar. Desalniettemin dient u "Rhinofebryl, harde
Risicominimalisatie materiaal voor voorschrijvers betreffende mycofenolaatbevattende
 Risicominimalisatie materiaal voor voorschrijvers betreffende mycofenolaatbevattende geneesmiddelen Dit risicominimalisatie materiaal voor mycofenolaat-bevattende geneesmiddelen is beoordeeld door het
Risicominimalisatie materiaal voor voorschrijvers betreffende mycofenolaatbevattende geneesmiddelen Dit risicominimalisatie materiaal voor mycofenolaat-bevattende geneesmiddelen is beoordeeld door het
BIJSLUITER 1. WAT IS DAFALGAN VOLWASSENEN 600 MG EN WAARVOOR WORDT HET GEBRUIKT?
 BIJSLUITER Lees de hele bijsluiter aandachtig door, omdat er voor u belangrijke informatie in staat. Raadpleeg uw arts of apotheker als u aanvullende vragen heeft. Bewaar deze bijsluiter, misschien heeft
BIJSLUITER Lees de hele bijsluiter aandachtig door, omdat er voor u belangrijke informatie in staat. Raadpleeg uw arts of apotheker als u aanvullende vragen heeft. Bewaar deze bijsluiter, misschien heeft
Nexavar - Sorafenib. Product Informatie Fiche. T +32(0) F +32(0) Campus Sint-Jan Schiepse bos 6.
 Nexavar - Sorafenib Product Informatie Fiche T +32(0)89 32 50 50 F +32(0)89 32 79 00 info@zol.be Campus Sint-Jan Schiepse bos 6 B 3600 Genk Campus Sint-Barbara Bessemerstraat 478 B 3620 Lanaken Medisch
Nexavar - Sorafenib Product Informatie Fiche T +32(0)89 32 50 50 F +32(0)89 32 79 00 info@zol.be Campus Sint-Jan Schiepse bos 6 B 3600 Genk Campus Sint-Barbara Bessemerstraat 478 B 3620 Lanaken Medisch
LORATADINE HOOIKOORTSTABLETTEN APOTEX 10 mg Module RVG Version Page 1 of 5 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER
 Version 2016-04 Page 1 of 5 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER loratadine Apotex hooikoortstabletten 10 mg, tabletten Loratadine Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken
Version 2016-04 Page 1 of 5 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER loratadine Apotex hooikoortstabletten 10 mg, tabletten Loratadine Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken
LORATADINE HOOIKOORTSTABLETTEN APOTEX 10 mg Module RVG Version 2017_12 Page 1 of 5 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER
 Version 2017_12 Page 1 of 5 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Loratadine Apotex hooikoortstabletten 10 mg, tabletten Loratadine Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken
Version 2017_12 Page 1 of 5 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Loratadine Apotex hooikoortstabletten 10 mg, tabletten Loratadine Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken
BIJSLUITER. PIL Isordil 5 20012016 0
 BIJSLUITER PIL Isordil 5 20012016 0 Bijsluiter: informatie voor de gebruiker Isordil 5, tabletten voor sublinguaal gebruik 5 mg isosorbidedinitraat Lees goed de hele bijsluiter voordat u dit geneesmiddel
BIJSLUITER PIL Isordil 5 20012016 0 Bijsluiter: informatie voor de gebruiker Isordil 5, tabletten voor sublinguaal gebruik 5 mg isosorbidedinitraat Lees goed de hele bijsluiter voordat u dit geneesmiddel
B. BIJSLUITER OSTEOMONO. 400 mg filmomhulde tablet
 B. BIJSLUITER OSTEOMONO 400 mg filmomhulde tablet Version:W.Somer.-15-5-2012 Page: 1 BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER. OSTEOMONO 400 mg filmomhulde tabletten glucosamine Lees de hele bijsluiter
B. BIJSLUITER OSTEOMONO 400 mg filmomhulde tablet Version:W.Somer.-15-5-2012 Page: 1 BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER. OSTEOMONO 400 mg filmomhulde tabletten glucosamine Lees de hele bijsluiter
BIJSLUITER. LIDOCAÏNE HCl 2% orale gel
 BIJSLUITER LIDOCAÏNE HCl 2% orale gel Lees de hele bijsluiter goed voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie in voor u. - Bewaar deze bijsluiter. Misschien heeft u
BIJSLUITER LIDOCAÏNE HCl 2% orale gel Lees de hele bijsluiter goed voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie in voor u. - Bewaar deze bijsluiter. Misschien heeft u
PATIENTENGIDS. Valproaat* Anticonceptie en zwangerschap: wat u moet weten
 PATIENTENGIDS Valproaat* Anticonceptie en zwangerschap: wat u moet weten Informatie voor meisjes en vrouwen die een medicijn gebruiken met de werkzame stof valproaat. Dit boekje is onderdeel van het valproaat
PATIENTENGIDS Valproaat* Anticonceptie en zwangerschap: wat u moet weten Informatie voor meisjes en vrouwen die een medicijn gebruiken met de werkzame stof valproaat. Dit boekje is onderdeel van het valproaat
Bijsluiter: informatie voor de patiënt. Neoclarityn 5 mg filmomhulde tabletten desloratadine
 Bijsluiter: informatie voor de patiënt Neoclarityn 5 mg filmomhulde tabletten desloratadine Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie in
Bijsluiter: informatie voor de patiënt Neoclarityn 5 mg filmomhulde tabletten desloratadine Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie in
Behandeling met ustekinumab. Risico minimalisatie materiaal: Veiligheidsinformatie betreffende ustekinumab voor patiënten
 Behandeling met ustekinumab Risico minimalisatie materiaal: Veiligheidsinformatie betreffende ustekinumab voor patiënten Belangrijke informatie Deze materialen beschrijven aanbevelingen om belangrijke
Behandeling met ustekinumab Risico minimalisatie materiaal: Veiligheidsinformatie betreffende ustekinumab voor patiënten Belangrijke informatie Deze materialen beschrijven aanbevelingen om belangrijke
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER
 Sandoz B.V. Page 1/6 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Entecavir Sandoz 0,5 mg, filmomhulde tabletten Entecavir Sandoz 1 mg, filmomhulde tabletten entecavir Lees goed de hele bijsluiter voordat
Sandoz B.V. Page 1/6 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Entecavir Sandoz 0,5 mg, filmomhulde tabletten Entecavir Sandoz 1 mg, filmomhulde tabletten entecavir Lees goed de hele bijsluiter voordat
Glucophage 500 bijsluiter 21-2-200127-2-2001 blz. 1 / 6
 Glucophage 500 bijsluiter 21-2-200127-2-2001 blz. 1 / 6 Glucophage 500, omhulde tabletten 500 mg Lees deze bijsluiter zorgvuldig door voordat u start met het gebruik van dit geneesmiddel. Bewaar deze bijsluiter,
Glucophage 500 bijsluiter 21-2-200127-2-2001 blz. 1 / 6 Glucophage 500, omhulde tabletten 500 mg Lees deze bijsluiter zorgvuldig door voordat u start met het gebruik van dit geneesmiddel. Bewaar deze bijsluiter,
RISICO MINIMALISATIE MATERIAAL BETREFFENDE TENOFOVIRDISOPROXIL-BEVATTENDE PRODUCTEN VOOR VOORSCHRIJVERS.
 RISICO MINIMALISATIE MATERIAAL BETREFFENDE TENOFOVIRDISOPROXIL-BEVATTENDE PRODUCTEN VOOR VOORSCHRIJVERS. Brochure controle nierfunctie bij behandeling van volwassenen met HIV De risico minimalisatie materialen
RISICO MINIMALISATIE MATERIAAL BETREFFENDE TENOFOVIRDISOPROXIL-BEVATTENDE PRODUCTEN VOOR VOORSCHRIJVERS. Brochure controle nierfunctie bij behandeling van volwassenen met HIV De risico minimalisatie materialen
CERITINIB (ZYKADIA ) KANKERCENTRUM. Onco_thor_022
 CERITINIB (ZYKADIA ) KANKERCENTRUM Onco_thor_022 WAT VINDT U TERUG IN DEZE BROCHURE / INHOUD(SOPGAVE) 01 Wat doet dit geneesmiddel? 3 02 Inname 3 03 Pletten / breken 3 04 Combinatie met andere geneesmiddelen
CERITINIB (ZYKADIA ) KANKERCENTRUM Onco_thor_022 WAT VINDT U TERUG IN DEZE BROCHURE / INHOUD(SOPGAVE) 01 Wat doet dit geneesmiddel? 3 02 Inname 3 03 Pletten / breken 3 04 Combinatie met andere geneesmiddelen
Risico-minimalisatiemateriaal betreffende Tasigna (nilotinib) voor voorschrijvers en apothekers
 Risico-minimalisatiemateriaal betreffende Tasigna (nilotinib) voor voorschrijvers en apothekers Introductie De risico-minimalisatiematerialen voor Tasigna (nilotinib) zijn beoordeeld door het College ter
Risico-minimalisatiemateriaal betreffende Tasigna (nilotinib) voor voorschrijvers en apothekers Introductie De risico-minimalisatiematerialen voor Tasigna (nilotinib) zijn beoordeeld door het College ter
Medicijnen na een TIA
 Medicijnen na een TIA Albert Schweitzer ziekenhuis september 2013 pavo 1072 Inleiding In deze folder leest u meer over medicijnen die vaak worden voorgeschreven na een TIA. Een TIA is een kortdurende beroerte
Medicijnen na een TIA Albert Schweitzer ziekenhuis september 2013 pavo 1072 Inleiding In deze folder leest u meer over medicijnen die vaak worden voorgeschreven na een TIA. Een TIA is een kortdurende beroerte
BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER
 Ikorel 10, tabletten 10 mg Ikorel 20, tabletten 20 mg nicorandil BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER Lees de hele bijsluiter zorgvuldig door voordat u start met het innemen van dit geneesmiddel.
Ikorel 10, tabletten 10 mg Ikorel 20, tabletten 20 mg nicorandil BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER Lees de hele bijsluiter zorgvuldig door voordat u start met het innemen van dit geneesmiddel.
Informatieboekje voor patiënten Wat u moet weten
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel VOLIBRIS. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel VOLIBRIS. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Duspatalin 135 mg omhulde tabletten mebeverinehydrochloride
 Versie 5.1 a MSP+MKT -032011 072013 012014-082014 Pagina 1/5 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER omhulde tabletten mebeverinehydrochloride Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat
Versie 5.1 a MSP+MKT -032011 072013 012014-082014 Pagina 1/5 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER omhulde tabletten mebeverinehydrochloride Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat
ETOS AMYLMETACRESOL PLUS DICHLOORBENZYLALCOHOL HONING & CITROEN zuigtabletten
 1.3.1 : Productinformatie Bladzijde: 1 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke zuigtablet bevat: Amylmetacresol 0,60 mg 2,
1.3.1 : Productinformatie Bladzijde: 1 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke zuigtablet bevat: Amylmetacresol 0,60 mg 2,
2. Wat u moet weten voordat u Paracetamol comp. Apotex gebruikt
 Version 2008_11 Page 1 of 5 1.3.1.3 PATIENT INFORMATION LEAFLET BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER PARACETAMOL COMP. APOTEX, TABLETTEN paracetamol en coffeïne Lees de hele bijsluiter zorgvuldig
Version 2008_11 Page 1 of 5 1.3.1.3 PATIENT INFORMATION LEAFLET BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER PARACETAMOL COMP. APOTEX, TABLETTEN paracetamol en coffeïne Lees de hele bijsluiter zorgvuldig
B. BIJSLUITER. KRUIDVAT GLUCOSAMINE 600 mg filmomhulde tablet
 B. BIJSLUITER KRUIDVAT GLUCOSAMINE 600 mg filmomhulde tablet Version:-21-8-2014 Page: 1 BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER. KRUIDVAT GLUCOSAMINE 600 mg filmomhulde tablet glucosamine Lees goed
B. BIJSLUITER KRUIDVAT GLUCOSAMINE 600 mg filmomhulde tablet Version:-21-8-2014 Page: 1 BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER. KRUIDVAT GLUCOSAMINE 600 mg filmomhulde tablet glucosamine Lees goed
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER. Lactulose EG 670 mg/ml, siroop Lactulose EG 10 g, poeder voor drank. lactulose
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Lactulose EG 10 g, poeder voor drank lactulose Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat innemen want er staat belangrijke informatie in voor
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Lactulose EG 10 g, poeder voor drank lactulose Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat innemen want er staat belangrijke informatie in voor
Additioneel risicominimalisatie-materiaal over de risico s van acitretine, alitretinoïne en isotretinoïne (orale retinoïden) voor voorschrijvers
 Additioneel risicominimalisatie-materiaal over de risico s van acitretine, alitretinoïne en isotretinoïne (orale retinoïden) voor voorschrijvers Dit materiaal beschrijft aanbevelingen om belangrijke risico
Additioneel risicominimalisatie-materiaal over de risico s van acitretine, alitretinoïne en isotretinoïne (orale retinoïden) voor voorschrijvers Dit materiaal beschrijft aanbevelingen om belangrijke risico
